Rajasthan Board RBSE Class 12 Chemistry Chapter 2 विलयन
RBSE Class 12 Chemistry Chapter 2 विलयन पाठ्यपुस्तक के अभ्यास प्रशन
RBSE Class 12 Chemistry Chapter 2 विलयन बहुचयनात्मक प्रश्न
RBSE Solutions For Class 12 Chemistry Chapter 2 प्रश्न 1.
500 g जल में 4g NaOH घुला है। विलयन की सान्द्रता होगी
(a) 8/L
(b) 0.2 N
(c) 0.2 m
(d) 0.2 M.
विलयन – Class 12 प्रश्न 2.
कौन-सा द्रव युग्म रॉउल्ट के नियम के धनात्मक विलचन प्रदर्शित करता है –
(a) जल + HCI
(b) 787 + HNO3
(c) बँजीन + मेथेनॉल
(d) ऐसीटोन + क्लोरोफार्म
RBSE Solutions For Class 12 Chemistry प्रश्न 3.
शुद्ध जल की मोलरता है-
(a) 55.5M
(b) 100 M
(c) 18 M
(d) 1 M.
प्रश्न 4.
निम्नलिखित 0.1M विलयनों को उनके क्वथनांक के बढ़ते क्रम। में व्यवस्थित कीजिए-
(i) NaCl
(ii)MgCl2
(iii) यूरिया
(iv) AlCl3
(a) (i) < (ii) < (iii) < (iv)
(b) (ii) < (i) < (i) < (iv)
(c) (iii) < (i) < (ii) < (iv)
(d) (iv) < (iii) < (ii) < (i)
प्रश्न 5.
यह एक आदर्श विलयन का गुण है-
(a) यह रॉउल्ट नियम को मानता है
(b) ∆H मिश्रण = 0
(c) ∆V मिश्रण = 0
(d) उपरोक्त सभी।
प्रश्न 6.
ताप बढ़ाने से किसी वस्तु का वाष्प दाब –
(a) सदैव बढ़ता है।
(b) घटता है।
(c) ताप पर निर्भर नहीं करता है।
(d) ताप पर आंशिक निर्भर करता है।
प्रश्न 7.
शर्करा 5% विलयन का परासरण दाब होगा
(a) 3.47 atm
(b) 5.07 atm
(c) 4.03 atm
(d) 2.09 atmm.
प्रश्न 8.
ताप बढ़ाने पर H2 गैस की जल में विलेयता –
(a) बढ़ती है।
(b) घटती है।
(c) अपरिवतर्तित रहती है।
(d) इनमें से कोई नहीं।
उत्तर:
- (c)
- (c)
- (a)
- (c)
- (d)
- (a)
- (a)
- (a)
RBSE Class 12 Chemistry Chapter 2 विलयन अति लघुतरात्मक प्रश्न
प्रश्न 1.
10% (\(\frac { w }{ W } \)) जलीय H2SO4 की मोललता की गणना कीजिए।
उत्तर:
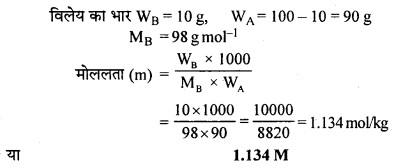
प्रश्न 2.
मोलरता किसे कहते हैं? इस पर ताप का प्रभाव लिखिए।
उत्तर:
एक लीटर विलयन में घुले हुए विलेय के मोलों की संख्या विलयन की मोलरता कहते हैं।
ताप का प्रभाव – ताप बढ़ाने से विलयन की मोलरता घट जाती है। क्योंकि ताप बढ़ाने से विलयन का आयतन बढ़ जाता है।
प्रश्न 3.
विलयन में किसी पदार्थ के मोल अंश को परिभाषित कीजिए।
उत्तर:
मिश्रण में किसी अवयव का मोल भिन्न मिश्रण में उस अवयव के मोल और मिश्रण के सभी अवयवों के कुल मोलों की संख्या को अनुपात होता है।
प्रश्न 4.
क्या गर्मियों में कार के रेडिएटरों में ऐथिलीन ग्लाइकॉल के प्रयोग की सलाह दी जाती है?
उत्तर:
नहीं, गर्मियों में कार के रेडिएटरों में ऐथिलीन ग्लाइकॉल की सलाह नहीं दी जाती है क्योंकि ऐथिलीन ग्लाइकॉल जल के हिमांक को कम कर देता है-जो सर्दियों में रेडिएटर में जल को जमने से रोकता है इसलिए इसकी सलाह सर्दियों में दी जाती है।
प्रश्न 5.
प्रतिलोम परासरण को परिभाषित कीजिए।
उत्तर:
यदि विलयन पर उसके परासरण दाब से अधिक दाब प्रयुक्त करें तो अर्द्धपारगम्य झिल्ली के माध्यम से विलयन से विलायक का बहाव शुद्ध विलायक की तरफ होने लगता है। इसे प्रतिलोम परासरण कहते हैं।
RBSE Class 12 Chemistry Chapter 2 विलयन लघुतरात्मक प्रश्न
प्रश्न 1.
ठोस की दूर्व में विलेयता पर ताप प्रभाव को स्पष्ट कीजिए। असामान्य अणु भार को सामान्य अणु भार से सम्बन्धित करने वाले वाण्टहॉफ गुणांक का सूत्र लिखिए। यह संगुणन व वियोजन क्रिया से किस प्रकार प्रभावित होता है ?
उत्तर:
ठोस की दृव में विलेयता पर ताप का प्रभाव –
संतृप्त विलयन में विलेय, ठोस एवं विलयन के मध्य निम्नांकित साम्य होता है।

ला-शातेलिए नियमानुसार यदि ∆H > 0 (शून्य) अर्थात् विलेय को विलायक में घोलने पर ऊष्मा अवशोषित होती है, तो ताप में वृद्धि पर ठोस विलेय की विलेयता में वृद्धि होगी।
उदाहरण – NH4Cl, KCl,AgNO3, NaNO3, Kl आदि।
यदि ∆H < 0 (शून्य) अर्थात् विलेय को विलायक में घोलने पर ऊष्मा मुक्त होती है तो ताप में वृद्धि पर ठोस विलेय की विलेयता में कमी होगी।
उदाहरण – NaOH, Li2SO4, (CH3COO)2 Ca आदि।
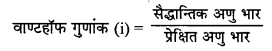
संगुणन होने की दशा में प्रेक्षित अणु भार बढ़ जाता है जिससे वाण्टहॉफ गुणांक का मान एक से कम (i < 1) हो जाता है तथा वियोजन होने पर प्रेक्षित अणु भार घट जाता है इसलिए वॉण्टहॉफ गुणांक का मान एक से अधिक (i > 1) हो जाता है।
प्रश्न 2.
आयनिक यौगिक AB का सैद्धान्तिक अणु भार एवं प्रेक्षित अणु भार क्रमशः 58.2 एवं 30 है। इसका वाण्टहॉफ गुणांक एवं वियोजन की मात्रा की गणना कीजिए।
उत्तर:
AB का सैद्धान्तिक अणु भार = 58.2
AB का प्रेक्षित अणु भार = 30

प्रश्न 3.
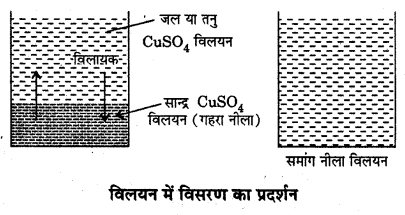
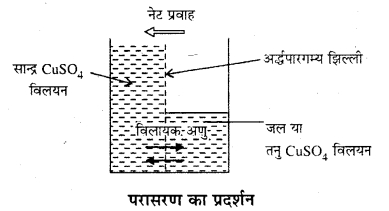
विसरण और परासरण में क्या अन्तर है? प्रत्येक का एक उदाहरण दीजिए। विसरण और परासरण क्रियाओं को नामांकित चित्र द्वारा दर्शाइए।
उत्तर:
विसरण और परासरण में अन्तर अनुच्छेद 2.10.4 (c) में देंखे।
प्रश्न 4.
एक प्रोटीन के 0.2L जलीय विलयन में 1.26 g प्रोटीन है। 300 K पर इस विलयन का परासरण दाब 2.57 × 10-3 bar पाया गया। प्रोटीन के मोलर द्रव्यमान का परिकलन कीजिए। (R = 0.0821 L bar mol-1 K-1)
उत्तर:

प्रश्न 5.
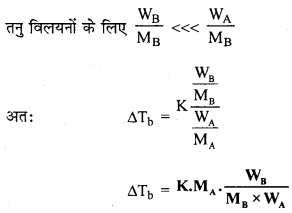
अवाष्पशील विलेय युक्त विलयन हेतु सिद्ध कीजिए –
∆Tb = Kb.m
उत्तर:

प्रश्न 6.
वाष्प दाब के अवनमन से अवाष्पशील पदार्थ का अणु भार कैसे ज्ञात किया जा सकता है ? इसे समझाइए।
उत्तर:
अवाष्पशील विलेय ठोस के लिए विलयन का आपेक्षिक वाष्प दाब अवनमन, विलेय की मोल भिन्न के समान होता है।

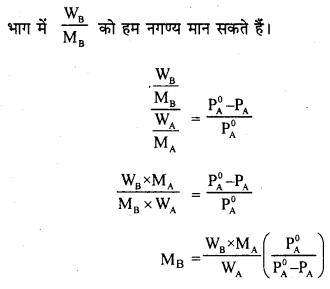
उपरोक्त समीकरण से अवाष्पशील विलेय का मोलर द्रव्यमान अर्थात् अणु भार ज्ञात किया जा सकता है यदि अन्य सभी राशि ज्ञात हो ।
प्रश्न 7.
गैसों की विलेयता से आप क्या समझते हैं? एक द्रव में गैसों की विलेयता को प्रभावित करने वाले कारक की व्याख्या कीजिए।
उत्तर:
गैसों की द्रवों में विलेयता – एक निश्चित ताप पर गैस की द्रवों में विलेयता एक निश्चित सीमा तक ही होती है। द्रव द्वारा गैस का अवशोषण करने पर गैस विलयन प्राप्त होता है। इसे गैस का अवशोषण भी कहते हैं। गैसों की द्रव में विलेयता को अवशोषण गुणांक द्वारा व्यक्त किया जाता है।
दुव-द्रव विलयन का वाष्य दाब – जब किसी द्रव (विलेय) का विलयन किसी द्रव (विलायक) में बनाया जाता है तो विलयन में दोनों अवयव वाष्पशील होते हैं। अत: विलयन के वाष्प दाब में दोनों अवयवों के वाष्प दाब का योगदान होता है।
माना कि किसी विलयन में दो वाष्पशील अवयव A व B उपस्थित हैं। इन अवयवों में आंशिक वाष्प दाब क्रमश: PA और PB हों तथा विलयन का वाष्प दाब P हो, तो –
P = PA + PB
प्रश्न 8.
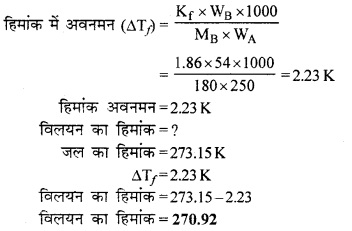
उस ताप की गणना कीजिए जिस पर 250 g जल में उपस्थित 54 g ग्लूकोज का विलयन जम जाएगा। (Kf = 1.86 K kg mol-1)
उत्तर:
दिया गया है –
विलेय का भार (WB) = 54g
विलेय का अणु भार (MB) = 180 g/mol
विलायक का भाग (WA) = 250 g
Kf = 1.86K kg mol-1
RBSE Class 12 Chemistry Chapter 2 विलयन अन्य महत्त्वपूर्ण प्रश्न
प्रश्न 1.
मेथेनॉल एक कार्बनिक यौगिक है फिर भी यह जल के साथ मुक्त रूप से मिश्रित हो जाता है, क्यों ?
उत्तर:
मेथेनॉल जल के साथ हाइड्रोजन बंध बनाता है। यही कारण है कि यह जल में मिश्रित हो जाता है।
प्रश्न 2.
विलयन की मोलरता पर ताप का क्या प्रभाव पड़ता है?
उत्तर:
ताप बढ़ाने पर मोलरता घट जाती है क्योंकि विलयन का आयतन ताप बढ़ाने पर बढ़ जाता है।
प्रश्न 3.
पेट्रोल तथा जल आपस में मिश्रित नहीं होते हैं, क्यों ?
उत्तर:
क्योंकि पेट्रोल अध्रुवी तथा जले ध्रुवी होता है।
प्रश्न 4.
निम्न पदों को परिभाषित करें –
- मोलरता
- मोलल उन्नयन स्थिरांक (Kb)
उत्तर:
- मोलरता – एक लीटर(1 dm3) विलयन में घुले हुए। विलेय के मोलों की संख्या को उस विलयन की मोलरता (M) कहते हैं।
- मोलल उन्नयन स्थिरांक – किसी विलायक का मोलल क्वथनांक उन्नयन स्थिरांक इसके क्वथनांक में उन्नयन के बराबर होता है, जब एक मोल विलेय 1000 g विलायक में घोला गया हो तो इसकी इकाई K kg mol-1 होती है।
प्रश्न 5.
विलयन में सभी अवयवों के मोल-अंशों का योग क्या होता है ?
उत्तर:
सभी अवयवों के मोल अंशों का योग एक होता है।
प्रश्न 6.
ppm क्या होता है ?
उत्तर:
विलेय के भार भागों की वह संख्या जो विलयन के एक मिलियन (106) भार भागों में उपस्थित हो, ppm कहलाती है।
प्रश्न 7.
मोलरता की तुलना में मोललता को वरीयता क्यों दी जाती है ?
उत्तर:
इसका कारण है कि मोललता पर ताप का कोई प्रभाव नहीं पड़त। एवं यह केवल द्रव्यमानों से सम्बन्धित होती है।
प्रश्न 8.
सोडियम कार्बोनेट के 20% जलीय विलयन से आप क्या समझते हैं ?
उत्तर:
सोडियम कार्बोनेट के 20% जलीय विलयन का अर्थ है कि 20 g सोडियम कार्बोनेट विलयन के 100 g में उपस्थित है। यहाँ विलायक का भार 80 g है।
प्रश्न 9.
विलयन, विलेय एवं विलायक को परिभाषित करें।
उत्तर:
दो या दो से अधिक यौगिकों को समांगी मिश्रण विलयन कहलाता है। इसमें जो अवयव अधिक मात्रा में प्रमुख रूप से उपस्थित होता है विलायक कहलाता है एवं जो अवयव कम मात्रा में होता है, विलेय कहलाता है।
प्रश्न 10.
मोल अंश को परिभाषित करें।
उत्तर:
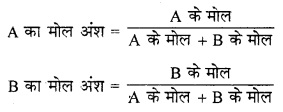
मोल अंश – मिश्रण में किसी अवयव का मोल अंश मिश्रण में उस अवयव के मोल और मिश्रण के सभी अवयवों के कुल मोलों की संख्या का अनुपात होता है।
अगर विलयन में दो अवयव A तथा B हैं तो
प्रश्न 11.
संतृप्त विलयन क्या होता है ?
उत्तर:
संतृप्त विलयन – ऐसा विलयन जिसमें एक निश्चित ताप पर और अधिक ठोस घोला न जा सके, संतृप्त विलयन कहलाता है।
प्रश्न 12.
विलयन कब ऊष्माक्षेपी अभिक्रिया प्रदर्शित करता
उत्तर:
जब विलेय तथा विलायक के मध्य आकर्षण बल, विलेय के अणुओं तथा विलायक के अणुओं के मध्य उपस्थित अन्तराआण्विक आकर्षण बल से अधिक हो तो अभिक्रिया ऊष्माक्षेपी होगी अर्थात् विलेय को विलायक में घोलने पर अभिक्रिया ऊष्मा का उत्सर्जन करेगी।
प्रश्न 13.
मोललता तथा मोलरता में अन्तर दें।
उत्तर:
मोललता तथा मोलरता में अन्तर
मोलरता –
- 1. 1 L विलयन में उपस्थित विलेय के मोलों की संख्या मोलरता कहलाती है।
- 2. इसकी इकाई mol/L है।
- 3. यह ताप के साथ परिवर्तित होती है।
मोललता –
- 1 kg विलायक में उपस्थित विलेय के मोलों की संख्या मोललता कहलाती है।
- इसकी इकाई molkg है।
- यह ताप के साथ अपरिवर्तित है।
प्रश्न 14.
क्या गैसों का मिश्रण सदैव विलयन को निरूपित करता
उत्तर:
हाँ, गैसों का मिश्रण सदैव विलयन को निरुपित करता है। क्योंकि इसकी प्रकृति समांगी होती है।
प्रश्न 15.
समान मोल के 1 M एवं 1 m जलीय विलयनों में से कौन-सा अधिक सान्द्रता का है ?
उत्तर:
1 M जलीय विलयन 1 m जलीय विलयन से अधिक सान्द्र होता है।
प्रश्न 16.
नॉर्मलता से आप क्या समझते हैं ?
उत्तर:
विलयन के एक लीटर में घुलित विलेय के ग्राम तुल्यांकों की संख्या नॉर्मलता कहलाती है। इसका मात्रक g eqiv. L-1 होता है।
प्रश्न 17.
ताप बढ़ने पर जल में NaCI की विलेयता बढ़ जाती है, क्यों ?
उत्तर:
क्योंकि NaCI के वियोजन की प्रकृति ऊष्माशोषी होती है।
प्रश्न 18.
समान विलेय के एक मोलर तथा एक मोलल जल विलयनों में से एक मोलर विलयन की सान्द्रता उच्च होती है, क्यों ?
उत्तर:
क्योंकि 1 मोलर विलयन का तात्पर्य है कि विलेय के 1 मोल 1000 ml विलयन में उपस्थित हैं अर्थात् इसमें विलायक की मात्रा 1000 ml से कम होती है जबकि 1 मोलल विलयन का तात्पर्य है कि 1000 g विलायक या 1000 ml विलायक में 1 मोल विलेय उपस्थित है। अतः 1 मोलर विलयन अधिक सान्द्र है।
प्रश्न 19.
ताँबे का सोने में विलयन किस प्रकार का विलयन है ?
उत्तर:
ठोस विलयन।
प्रश्न 20.
अमलगम किस प्रकार का विलयन होता है?
उत्तर:
ठोस विलयन।
प्रश्न 21.
कर्पूर का नाइट्रोजन गैस में विलयन किस प्रकार का विलयन है ?
उत्तर:
ठोस विलयन।
प्रश्न 22.
जल में घुली ऑक्सीजन किस प्रकार का विलयन है ?
उत्तर:
द्रव विलयन।
प्रश्न 23.
आदर्श विलयन किन्हें कहते हैं ?
उत्तर:
दो विलायकों के मिश्रण प्राप्त करने हेतु भिन्न-भिन्न प्रतिशत मात्रा मिलाने पर प्रयोगात्मक वाष्प दाब यदि रॉउल्ट नियम के द्वारा निर्गत वाष्प दाबों के मानों के बराबर आता है तो वे आदर्श विलयन कहलाते हैं।
प्रश्न 24.
मिश्रणीय द्रव युग्म प्रायः रॉउल्ट नियम से ऋण अथवा धन विचलन दिखाते हैं, क्यों ?
उत्तर:
यदि मिश्रणीय द्रव युग्मों का वाष्प दाब रॉउल्ट नियम के वाष्पदाब से अधिक होता है तो इसे धन विचलन कहते हैं तथा यदि प्रयोगात्मक वाष्प दाब कम आता है तो उसे ऋण विचलन कहते हैं।
प्रश्न 25.
किस प्रकार के द्रव आदर्श विलयन बनाते है?
उत्तर:
अत्यधिक तनु विलयन, समान संरचना तथा ध्रुवणता वाले द्रव आदर्श विलयन बनाते हैं।
प्रश्न 26.
दो द्रव X तथा Y का क्वथनांक क्रमशः 100°C तथा 120°C है। इनमें से किस द्रव का वाष्प दाब 60°C पर अधिक होगा ?
उत्तर:
द्रव का क्वथनांक जितना कम होता है उतना अधिक द्रव वाष्पशील होता है। अत: द्रव X का वाष्प दाब 60°C पर अधिक होगा।
प्रश्न 27.
किसी विलयन का वाष्प दाब उसके विलायक की अपेक्षा कम क्यों होता है ?
उत्तर:
किसी अवाष्पशील विलेय को मिलाने पर विलायक का कुछ स्थान विलेय के अणुओं द्वारा घेर लिया जाता है जिस कारण से वाष्प का बनना कम हो जाता है फलतः वाष्प दाब भी कम हो जाता है।
प्रश्न 28.
ऐथेनॉल तथा साइक्लोहेक्सेन का विलयन धनात्मक विचलन क्यों प्रदर्शित करता है?
उत्तर:
विलयन में विलेय तथा विलायक के मध्य अन्त:क्रियाएँ विलेय-विलेय के अणुओं तथा विलायक-विलायक के अणुओं के मध्य अन्त:क्रियाओं के सापेक्ष कम होती हैं अर्थात् जब साइक्लोहेक्सेन को एथेनॉल में मिलाते हैं तो ऐथेनॉल के हाइड्रोजन बन्ध टूट जाते हैं जिस कारण ये धनात्मक विचलन प्रदर्शित करते हैं।
प्रश्न 29.
रॉउल्ट का नियम किन स्थितियों में लागू नहीं होता ?
उत्तर:
विलेय के वियोजन या संगुणन प्रवृत्ति होने पर रॉउल्ट का नियम लागू नहीं होता है।
प्रश्न 30.
आदर्श विलयन की विशेषता लिखें।
उत्तर:
- ये रॉउल्ट के नियम का पालन करते हैं।
- ∆H मिश्रण = 0
- ∆V मिश्रण = 0
प्रश्न 31.
यदि कोई विलेय ऊष्माशोषी प्रक्रम द्वारा विलयन बनाता है तो ऐसे विलयन का ताप बढ़ाने से विलेयता पर क्या प्रभाव पड़ता
उत्तर:
ला-शातेलिये नियम के अनुसार यदि अभिक्रिया ऊष्माशोषी है तो ताप बढ़ाने से विलेय की विलेयता बढ़ जाती है।
प्रश्न 32.
क्या हम स्थिर क्वाथी मिश्रण के यौगिकों को प्रभाजी आसवन द्वारा पृथक् कर सकते है? समझाइये।
उत्तर:
नहीं, क्योंकि स्थिर क्वाथी मिश्रण में दोनो अवयव समान ताप पर उबलते हैं। अतः हम उन्हें पृथक नहीं कर सकते।
प्रश्न 33.
द्रव A तथा B मिश्रित करने पर गर्म विलयन बनाते हैं। बताइये कि ये रॉउल्ट नियम से किस प्रकार का विचलन प्रदर्शित करेंगे ?
उत्तर:
विलयन गर्म हो जाता है अर्थात् ∆Hmix = -ve. अतः ये ऋणात्मक विचलन प्रदर्शित करेंगे।
प्रश्न 34.
द्रव A तथा B मिश्रित किये जाने पर ठंडा विलयन बनाते हैं। बताइये कि ये रॉउल्ट नियम से किस प्रकार का विचलन प्रदर्शित करेंगे।
उत्तर:
विलयन ठंडा हो जाता है अर्थात् ∆Hmix = +ve अतः ये धनात्मक विचलन प्रदर्शित करेंगे।
प्रश्न 35.
आदर्श विलयन के लक्षण लिखें।
उत्तर:
- रॉउल्ट के नियम का पालन करते हैं।
- इन्हें प्रभाजी आसवन से पृथक नहीं कर सकते।
- ∆Hmix = 0
- ∆Vmix = 0
प्रश्न 36.
क्लोरोफार्म तथा ऐसीटोन को मिलाने पर ऊष्मा उत्सर्जित क्यों होती है ?
उत्तर:
क्योंकि दोनों के मध्य आकर्षण बल अत्यधिक बढ़ जाता है। जिस कारण ऊष्मा उत्सर्जित होती है।
प्रश्न 37.
रेफ्रीजरेटर से निकालकर प्याज काटना साधारण ताप पर रखी प्याज को काटने की अपेक्षा ज्यादा आरामदायक है, क्यों?
उत्तर:
कम ताप पर वाष्प दाब कम होता है जिससे आँसू लाने वाले पदार्थ की वाष्प कम ताप पर कम बनती है। अतः आरामदायक होता है।
प्रश्न 38.
हेनरी का नियम समझाइये।
उत्तर:
हेनरी का नियम-किसी द्रव में गैस की विलेयता गैस के दाब के समानुपाती होती है। अर्थात्
गैस का आंशिक दाब ‘p’ ∝ गैस के मोल अंश (x)
p ∝ x p = KH.x
KH = हेनरी नियतांक
प्रश्न 39.
अमोनिया की बोतलों को खोलने से पहले ठंडा करते हैं क्यों ?
उत्तर:
ठंडा करने से वाष्प दाब घट ज़ाता है और द्रव अमोनिया एक साथ बोतल से स्वयं बाहर नहीं निकलती है।
प्रश्न 40.
वाष्प दाब अवनमन के लिये रॉउल्ट का नियम लिखें।
उत्तर:
अवाष्पशील विलेय के विलयन का वाष्प दाब, विलायक के वाष्प दाब से कम होता है अतः रॉउल्ट के अनुसार, “एक निश्चित ताप पर अवाष्पशील विलेय युक्त विलयन के लिये आपेक्षिक वाष्प दाब अवनमन विलेय के मोल भिन्न के बराबर होता है।”
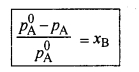
प्रश्न 41.
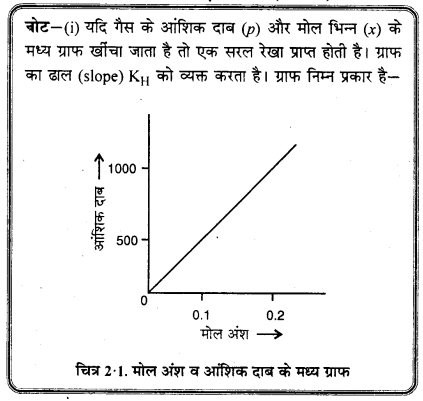
समान ताप पर ऑक्सीजन जल में हाइड्रोजन से ज्यादा । विलेय है। इनमें से किसका KH मान अधिक होगा?
उत्तर:
![]()
अतः हाइड्रोजन गैस का हेनरी नियतांक अधिक होगा।
प्रश्न 42.
विलेय के आपेक्षिक वाष्प दाब अवनमन एवं अवाष्पशील विलेय के अणु भार में सम्बन्ध दीजिए।
उत्तर:
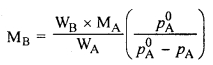
प्रश्न 43.
जल के वाष्प दाब पर क्या प्रभाव पड़ेगा यदि इसमें एक चम्मच नमक मिला दें?
उत्तर:
जल का वाष्प दाब कम हो जायेगा।
प्रश्न 44.
कार्बोनेटीकृत शीतल पेय की ठण्डी बोतल को खोलने पर गैस के बुलबुले बाहर निकलते हैं। समझाइये।
उत्तर:
शीतल पेय की ठण्डी बोतल में उच्च दाब पर CO2 भरी होती है। जब ढक्कन खोलते हैं तो CO2 गैस उच्च दाब वाले क्षेत्र से निम्न दाब वाले क्षेत्र की ओर तेजी से जाती है। इसी कारण बुलबुले निकलते दिखाई देते हैं।
प्रश्न 45.
प्रेशर कुकर के प्रयोग से कुकिंग का समय घट जाता है, क्यों ?
उत्तर:
क्योंकि द्रव के ऊपर उच्चदाब होने पर द्रव का ताप अधिक हो जाता है जिससे कुकिंग का समय घट जाता है।
प्रश्न 46.
ताप बढ़ाने पर हेनरी स्थिरांक पर क्या प्रभाव पड़ता है?
उत्तर:
ताप बढ़ाने पर हेनरी स्थिरांक का मान बढ़ जाता है।
प्रश्न 47.
हेनरी स्थिरांक एवं गैसों की द्रवों में विलेयता में क्या सम्बन्ध है ?
उत्तर:
हेनरी स्थिरांक का मान जितना अधिक होगा गैसों की द्रवों में विलेयता उतनी ही कम होगी।
प्रश्न 48.
जलीय स्पीशीज के लिये गर्म जल की तुलना में ठंडे जल में रहना अधिक आरामदायक होता है क्यों ?
उत्तर:
ताप बढ़ने पर गैसों की विलेयता कम हो जाती है अतः गर्म जल में ऑक्सीजन की विलेयता कम होती है जबकि ठंडे जल में अधिक। अतः जलीय स्पीशीज ठंडे जल में ज्यादा रहना पसंद करती हैं।
प्रश्न 49.
ऐनॉक्सिया क्या है?
उत्तर:
ऐनॉक्सिया ऊँचाई वाली जगहों पर रहने वाले लोगों में पायी जाने वाली एक बीमारी है। इसमें लोग स्पष्टतया सोच नहीं पाते एवं कमजोर हो जाते हैं क्योंकि ऊँचाई वाली जगह पर दाब कम होता है। जिसके कारण रुधिर और ऊतकों में ऑक्सीजन की सान्द्रता निम्न हो जाती है।
प्रश्न 50.
गोताखोरों द्वारा ले जाये जाने वाले ऑक्सीजन टैंकों में क्या होता है ?
उत्तर:
गोताखोरों द्वारा ले जाये जाने वाले ऑक्सीजन टैंकों में 11-7% हीलियम, 56:2% नाइट्रोजन तथा 32.1% ऑक्सीजन होती है।
प्रश्न 51.
मोलल उन्नयन स्थिरांक अथवा मोलल हिमांक स्थिरांक किसी एक विलायक के लिये निश्चित मान होते हैं, क्यों ?
उत्तर:
मोलल उन्नयन (अथवा हिमांक) स्थिरांक K का मान निम्न सूत्र द्वारा दिया जा सकता है।

चूँकि T एवं l के मान किसी विलायक के लिये निश्चित होते हैं। अतः K का मान भी विलायक के लिये निश्चित होता है।
प्रश्न 52.
जल में सोडियम क्लोराइड घोलने से जल के क्वथनांक पर क्या प्रभाव पड़ता है ?
उत्तर:
चूँकि जल में नमक घोलने पर नमक के अणु जल की सतह का कुछ भाग घेर लेते हैं अतः वाष्पन के लिये उपलब्ध आपेक्षिक पृष्ठ सतह कम हो जाती है जिससे वाष्पन कम हो जाता है जिसके कारण क्वथनांक बढ़ जाता है।
प्रश्न 53.
क्वथनांक उन्नयन या हिमांक अवनमन की विधि से अणु भार ज्ञात करने में साधारण थर्मामीटर का उपयोग क्यों नहीं किया जाता है ?
उत्तर:
क्योंकि क्वथनांक में उन्नयन तथा हिमांक में अवनमन बहुत कम होता है। अतः हमें 0-01°C की लघुतम माप का थर्मामीटर की आवश्यकता होती है। ऐसा थर्मामीटर बैकमान ने बनाया था जिसे बैकमान थर्मामीटर कहते हैं।
प्रश्न 54.
परासरण से आप क्या समझते हैं ?
उत्तर:
परासरण – जब विलायक के अणु अर्द्धपारगम्य झिल्ली द्वारा निम्न सान्द्रता वाले विलयन से उच्च सन्द्रिता वाले विलयन की तरफ गमन करते हैं तो इस प्रक्रिया को परासरण (Osmosis) कहते हैं।
प्रश्न 55.
परासरण दाब किसे कहते हैं ?
उत्तर:
परासरण दाब – उच्च सान्द्रता वाले विलयन पर लगाया गया बाह्य दाब जो विलायक के अणुओं का प्रवाह अर्द्धपारगम्य झिल्ली से रोक दे, परासरण दाब (Osmotic Pressure) कहलाता है।
प्रश्न 56.
अर्द्धपारगम्य झिल्ली क्या होती है ? उदाहरण दें ?
उत्तर:
अर्द्धपारगम्य झिल्ली – वह झिल्ली जो विलायक के अणुओं को गुजर जाने दे, परन्तु विलेय के अणुओं को नहीं, अर्द्धपारगम्य झिल्ली कहलाती है।
उदाहरण – अण्डे की झिल्ली, चर्म पत्र आदि।
प्रश्न 57.
प्रतीप परासरण या प्रतिलोम परासरण किसे कहते हैं ?
उत्तर:
प्रतीप परासरण – यदि उच्च सान्द्रता वाले विलयन की तरफ परासरण दाब से अधिक दाब का प्रयोग करें तो विलायक अधिक सान्द्रता वाले विलयन से अर्द्धपारगम्य झिल्ली द्वारा निम्न सान्द्रता वाले विलयन की तरफ प्रवाहित होने लगता है। इस प्रक्रिया को प्रतीप परासरण कहते हैं।
प्रश्न 58.
हिमांक (Freezing Point) से आप क्या समझते हैं ?
उत्तर:
हिमांक – वह ताप जिस पर किसी द्रव की द्रव एवं ठोस अवस्थाओं का वाष्प दाब समान हो जाता है, वह उस द्रव का हिमांक कहलाता है।
प्रश्न 59.
मोलल उन्नयन स्थिरांक से आप क्या समझते हैं ?
उत्तर:
मोलल उन्नयन स्थिरांक – क्वथनांक में होने वाला उन्नयन, जब एक अवाष्पशील विलेय का 1 मोल विलायक के 1000 g में घुला हो, मोलल उन्नयन स्थिरांक कहलाता है। इसका मात्रक K kg mol-1 है।
प्रश्न 60.
मोलल अवनमन स्थिरांक से आप क्या समझते हैं ?
उत्तर:
मोलल अवनमन स्थिरांक – हिमांक में होने वाला अवनमन, जब एक अवाष्पशील विलेय का 1 मोल विलायक के 1000.g में घुला हो, मोलल अवनमन स्थिरांक कहलाता है। इसका मात्रक K kg mol-1 होता है।
प्रश्न 61.
क्या होता है जब हम रक्त कोशिका को जल (अल्प परासारी विलयन में रखते हैं? कारण दीजिये।
उत्तर:
रक्त कोशिका फूल जाती है, क्योंकि जल के अणु परासरण के द्वारा कम सान्द्रता वाले (जल से) अधिक सान्द्रता वाले (रक्त कोशिका) विलयन की तरफ प्रवाह करते हैं।
प्रश्न 62.
प्रतिहिम (Antifreeze) क्या होता है ?
उत्तर:
प्रतिहिम – वह पदार्थ जो जल में मिलाने पर जल के हिमांक को कम कर देता है, प्रतिहिम कहलाता है। जैसे-ऐथिलीन ग्लाइकॉल (Ethylene glycol)
प्रश्न 63.
क्वथनांक की उन्नयन विधि से किसी वाष्पशील पदार्थ का अणु भार क्यों नहीं ज्ञात कर सकते हैं ?
उत्तर:
क्योंकि यह विधि केवल अवाष्पशील विद्युत् अपघट्यों के लिये ही उपयुक्त है। वाष्पशील पदार्थ के विलयन को गर्म करने पर वाष्पशील पदार्थ पृथक् हो जाते हैं।
प्रश्न 64.
किसी द्रव में अवाष्पशील पदार्थ डालने पर उसके क्वथनांक में उन्नयन क्यों होता है ?
उत्तर:
क्वथनांक – वह ताप जिस पर द्रव का वाष्प दाब वायुमण्डलीय दाब के बराबर हो जाये, क्वथनांक कहलाता है।
द्रव में अवाष्पशील पदार्थ डालने पर द्रव का वाष्प दाब कम हो जाता है, जिस कारण वाष्पदाब तथा वायुमण्डलीय दाब का अन्तर काफी बढ़ जाता है, फलतः हमें विलयन के वाष्प दाब को वायुमण्डलीय दाब के बराबर करने के लिये उसे अधिक ताप देना पड़ता है। जिस कारण उसका क्वथनांक बढ़ जाता है यही क्वथनांक में उन्नयन कहलाता है।
प्रश्न 65.
समपरासारी विलयन क्या होते हैं ?
उत्तर:
समपरासारी विलयन – ऐसे विलयन जिनका परासरण दाब समान ताप पर समान हो, समपरासारी विलयन (isotonic solutions) कहलाते हैं। इनकी मोलर सान्द्रता समान होती है।
एवं ये अर्द्धपारगम्य झिल्ली द्वारा परासरण की प्रक्रिया को प्रदर्शित नहीं करते हैं।’
प्रश्न 66.
NaCl, CaCl2, CaF2, आदि को बर्फ से ढकी सड़कों को साफ करने में प्रयुक्त करते हैं, क्यों?
उत्तर:
NaCl, CaCl2, CaF2 आदि विहिमीकारक पदार्थ का कार्य करते हैं अर्थात् जल के हिमांक को कम कर देते हैं जिससे यह जमकर बर्फ नहीं बन पाता है। इसी कारण जब इन्हें सड़कों पर छिड़कते हैं तो बर्फ गल जाती है और रास्ता साफ हो जाता है।
प्रश्न 67.
जल का मोलल अवनमन स्थिरांक 1.86 Kkg mol-1 है, इसका क्या अर्थ होता है ?
उत्तर:
मोलल अवनमन स्थिरांक का यह मान दर्शाता है कि जब अवाष्पशील पदार्थ के 1 मोल को 1000 g विलायक में घोलते हैं तो इसका हिमांक 1.86 K कम हो जाता है।
प्रश्न 68.
अण्डे के बाह्य कवच को हटाकर यदि उसे निम्न में रखें तो क्या होगा –
- आसुत जल में
- NaCI के संतृप्त विलयन में ?
उत्तर:
- आसुत जल में – यहाँ अण्डा अंत: परासरण प्रदर्शित करेगा और वह फूल जायेगा।
- NaCl के संतृप्त विलयन में – यहाँ अण्डा बाह्य परासरण प्रदर्शित करेगा और सिकुड़ जायेगा।
प्रश्न 69.
किसी पदार्थ का गलनांक उसमें उपस्थित अशुद्धियों के सम्बन्ध में किस प्रकार जानकारी देता है? बताएँ।
उत्तर:
अशुद्धियाँ किसी भी द्रव में विलेय का कार्य करती हैं। ज्यादा अशुद्धियाँ किसी भी पदार्थ के हिमांक को अधिक अवनमित कर देती हैं अर्थात् हिमांक में ज्यादा अवनमन किसी विलायक में ज्यादा अशुद्धियों की उपस्थिति की जानकारी देता है।
प्रश्न 70.
अणुसंख्यक गुणधर्म से आप क्या समझते हैं?
उत्तर:
अणुसंख्यक गुणधर्म – वे गुणधर्म जो कि विलेय के कणों की संख्या पर निर्भर करते हैं, परन्तु विलेय की प्रकृति पर नहीं, अणुसंख्यक गुणधर्म (Colligative properties) कहलाते हैं।
प्रश्न 71.
अणुसंख्यक गुणधर्म कितने प्रकार के होते हैं?
उत्तर:
ये निम्न प्रकार के होते हैं –
- क्वथनांक में उन्नयन
- हिमांक में अवनमन
- वाष्पदाब में कमी
- परासरण दाब ।
प्रश्न 72.
जल में चीनी या नमक मिलाने से जल का क्वथनांक क्यों बढ़ जाता है ?
उत्तर:
जब किसी अवाष्पशील विलेय को जल में मिलाते हैं तो जल का वाष्प दाब घट जाता है क्योंकि कुछ विलेय के कण विलायक की सतह को घेर लेते हैं जिसके कारण वाष्प दाब कम हो जाता है। वाष्प दाब को वायुमण्डलीय दाब के बराबर करने के लिये उसे अधिक ताप देना होता है, जिस कारण क्वथनांक बढ़ जाता है।
प्रश्न 73.
जल में NaCI घोलने पर विलयन के हिमांक पर क्या प्रभाव पड़ता है ?
उत्तर:
जल में नमक घोलने पर नमक के अणु जल की सतह का कुछ भाग घेर लेते हैं अतः वाष्पन के लिये उपलब्ध आपेक्षिक पृष्ठ सतह कम हो जाती है। इसके फलस्वरूप वाष्पन कम होता है अत: हिमांक कम हो जाता है।
प्रश्न 74.
प्रेशर कुकर में पानी देर में उबलता है, पर दाल जल्दी गल जाती है। क्यों ?
उत्तर:
प्रेशर कुकर में दाब अधिक होने के कारण पानी का वाष्प दाब देर में बाह्य दाब के बराबर होता है अर्थात् अधिक दाब पर पानी का क्वथनांक बढ़ जाता है और पानी 100°C से अधिक ताप पर उबलता है। 100°C से अधिक ताप पर रखी दाल को अधिक ऊष्मा प्राप्त होती है। अतः जल्दी गलती है।
प्रश्न 75.
एक रसोइया प्याज को साधारण ताप पर काटने की जगह शीतल किये प्याज को काटने पर कम आँसू बहाता है। क्यों ?
उत्तर:
प्याज को ठंडा करके काटने पर प्याज में उपस्थित वाष्पशील द्रवों का वाष्पन कम होता है। अतः रसोइए की आँख तक कम द्रव वाष्पित होकर जाता है और उसे जलन कम होती है।
प्रश्न.76.
जल में ऐसीटोन घोलने पर उसके क्वथनांक पर क्या प्रभाव पड़ेगा ?
उत्तर:
ऐसीटोन वाष्पशील द्रव है अत: विलयन का क्वथनांक जल एवं ऐसीटोन के क्वथनांकों के मानों के बीच रहेगा।
प्रश्न 77.
अजलीय विलयनों के परासरण दाब को प्रयोगात्मक रूप से ज्ञात करने की विधि कौन-सी है ?
उत्तर:
टाउनसेंड विधि।
प्रश्न 78.
बर्फ पर नमक छिड़कने से बर्फ जल्दी गलती है, क्यों ?
उत्तर:
नमक मिलाने पर बर्फ का गलनांक कम हो जाता है, परन्तु वातावरण को तापक्रम अधिक ही रहता है। अतः बर्फ जल्दी पिघल जाती है।
प्रश्न 79.
कार्बनिक प्रकृति की कृत्रिम अर्द्ध-पारगम्य झिल्ली का कार्य कौन करता है ?
उत्तर:
फीनॉल का तल।
प्रश्न 80.
किन्हीं दो अकार्बनिक प्रकृति की कृत्रिम अर्द्ध-पारगम्य झिल्लियों के नाम लिखो।
उत्तर:
- श्लेष्मायुक्त कॉपर फेरोसायनाइड
- श्लेष्मायुक्त कैल्सियम फॉस्फेट।
प्रश्न 81.
हिमांक अवनमन विधि से किसी अवाष्पशील पदार्थ का अणुभार ज्ञात करने का सूत्र लिखो ?
उत्तर:
किसी अवाष्पशील पदार्थ का अणुभार निम्नलिखित सूत्र द्वारा ज्ञात कर सकते हैं –

प्रश्न 82.
जल वाष्प दाब क्या होगा यदि एक चम्मच चीनी उसमें डाल दी जाये?
उत्तर:
जल का वाष्प दाब घट जायेगा।
प्रश्न 83.
क्वथनांक उन्नयन विधि से किसी अवाष्पशील पदार्थ का अणु भार ज्ञात करने का सूत्र लिखो?
उत्तर:
क्वथनांक उन्नयन विधि से किसी अवाष्पशील पदार्थ का अणुभार निम्न सूत्र द्वारा ज्ञात कर सकते हैं –

प्रश्न 84.
किसी विलयन के परासरण दाब एवं उसके अणु भार में क्या सम्बन्ध है ?
उत्तर:

प्रश्न 85.
आइसोप्रोपिल ऐल्कोहॉल को रगड़ने से प्रायः शीतलन (cooling sensation) उत्पन्न होता है, क्यों?
उत्तर:
आइसोप्रोपिल ऐल्कोहॉल एक वाष्पशील द्रव है जिसके कारण त्वचा पर रखने पर ये आवश्यक वाष्पन की गुप्त ऊष्मा को अवशोषित कर लेता है, जिससे शीतलन उत्पन्न होता है।
प्रश्न 86.
उस यौगिक को वाण्टहॉफ गुणांक कितना होगा जो कि विलायक की उपस्थिति में चतुर्थयन (tetramerisation) करता है ?
उत्तर:
इसके वाण्टहॉफ गुणांक का मान (i) = 0.25 होगा, क्योंकि विलेय का प्रेक्षित मोलर द्रव्यमान उसके सामान्य मोलर द्रव्यमान का चार गुना होगा।
प्रश्न 87.
गर्मी के दिनों में कार के रेडिएटरों में एथिलीन ग्लाइकॉल का प्रयोग क्यों किया जाता है ?
उत्तर:
एथिलीन ग्लाइकॉल जल के हिमांक को बहुत कम कर देता है और प्रति हिम की भाँति कार्य करता है। यह अत्यधिक गर्मी में भी इंजन को शीतल रखता है इस कारण से गर्मी के दिनों में कार के रेडिएटरों में ऐथिलीन ग्लाइकॉल का प्रयोग करते हैं।
प्रश्न 88.
C6H12O6, LiCl, Na2SO4 एवं K4 [Fe(CN)6] के सममोलर विलयनों के क्वथनांक एवं हिमांक का घटता हुआ क्रम क्या होगा ?
उत्तर:
(i) क्वथनांक का उन्नयन (∆Tb) ∝ विलेय में कणों की संख्या अर्थात् कणों की संख्या जितनी अधिक होगी, क्वथनांक में उन्नयन भी उतना अधिक होगी।
अतः,
क्वथनांक – K4[Fe(CN)6] > Na2SO4 > LiCl > C6H12O6
(ii) हिमांक में अवनमन ∝ विलेय के कणों की संख्या
अतः, हिमांक का क्रम C6H12O6 > LiCl > Na2SO4 > K4 [Fe(CN)6]
प्रश्न 89.
K3[Fe(CN)6] के वाण्टहॉफ गुणांक का मान क्या होगा ?
उत्तर:
K3[Fe(CN)6] → 3K+ +[Fe(CN)6]3-
अतः इसका वाण्ट हॉफ गुणांक = 4
प्रश्न 90.
निम्नलिखित विलयनों को वाण्टहॉफ गुणांक के बढ़ते क्रम में व्यवस्थित कीजिए।
0.1 M CaCl2, 0.1M KCl, 0.1 M Al2 (SO4)3, 0.1 M C12 H22 O11
उत्तर:
0.1M C12H22,O11 < 0.1 M KCl < 0.1 M CaCl2 < 0.1 MAl2 (SO4)3
प्रश्न 91.
जल में Al2(SO4)3 के तनु विलयन के लिये वाण्टहॉफ गुणांक का मान क्या होगा ?
उत्तर:
तनु विलयन में Al2(SO4)3 वियोजित हो जाता है।
Al2(SO4)3 → 2Al3+ + 3sO42-

प्रश्न 92.
लवणों के असामान्य या अपसामान्य अणु भार से आप क्या समझते हैं ?
उत्तर:
यदि तनु विलयन में विलेय का वियोजन या संगुणन होता है तो विलेय का अणु भार उसके वास्तविक अणु भार से भिन्न आता है। इस अणु भार को ही असामान्य या अपसामान्य (Abnormal) अणु भार कहते हैं।
प्रश्न 93.
वाण्टहॉफ गुणांक को परिभाषित करें।
उत्तर:
वाण्टहॉफ गुणांक विलेय के वियोजन या संगुणन के सम्बन्ध में जानकारी देता है। यदि
i = 1 विलेय न हो संगुणित होता है न ही वियोजित
i > 1 विलेय यहाँ वियोजित होता है।
i < 1 विलेय यहाँ संगुणित होता है।
प्रश्न 94.
1 मोलर ग्लूकोज, 1 मोलर KCl तथा 1 मोलर K2SO4 में किसका हिमांक सबसे कम होगा और क्यों ?
उत्तर:
यहाँ K2SO4 का हिमांक सबसे कम होगा, क्योंकि यह तीन कणों में वियोजित होता है।
प्रश्न 95.
तनु विलयन के लिये वाण्टहॉफ समीकरण क्या होता है?
उत्तर:
यदि तनु विलयन में विलेय वियोजित या संगुणित होता है। तो इनके अणु भार अपसामान्य निकलते हैं। इनके अपसामान्य अणु भारों को तथा अणुसंख्यक गुणों को स्पष्ट करने के लिये वाण्टहॉफ ने एक गुणांक दिया जिसे वाण्टहॉफ गुणांक ” कहते हैं। इसके अनुसार,

प्रश्न 96.
जल के क्वथनांक में उन्नयन निम्नलिखित दो स्थितियों में भिन्न क्यों होता है –
(a) 0.1 मोलल KCI विलयन?
(b) 0.1 मोलल यूरिया विलयन?
उत्तर:
KCl विलयन एक विद्युत् अपघट्य है। यह विलयन में वियोजित होता है तथा दो आयन K+ तथा Cl– देता है। यूरिया विलयन विद्युत् अनअपघट्य हैं और वियोजित नहीं होता है। यही कारण है कि दोनों ही स्थितियों में क्वथनांक में उन्नयन भिन्न होता है।
प्रश्न 97.
निम्नलिखित विलयनों में से किसको परासरण दाब अधिक है और क्यों –
(i) 0.1 M ग्लूकोस विलयन?
(ii) 0.1 M NaCl विलयन?
(iii) 0.1 M K2SO4 विलयन?
(iv) 0.1 MAl2(SO4) विलयन?
उत्तर:
0.1 MAl2(SO4)3 विलयन का परासरण दाब सबसे अधिक होता है क्योंकि यह विलयन में वियोजित होकर 5 कणों को अर्थात् तीन SO42- आयन तथा दो Al3+ आयन देता है। अणुसंख्य गुणधर्म आयनों की संख्या पर निर्भर करता है।
अणुसंख्यक गुणधर्म α अणुओं की संख्या
RBSE Class 12 Chemistry Chapter 2 विलयन लघु उत्तरीय प्रश्न
प्रश्न 1.
गैसों की विलेयता से आप क्या समझते हैं ? विलेयता को प्रभावित करने वाले कारक लिखें।
उत्तर:
गैसों की विलेयता – एक निश्चित ताप एवं एक निश्चित वायुमण्डलीय दाब पर विलायक के एक इकाई आयतन में घुली गैस का NTP पर आयतन उसका अवशोषण गुणांक होता है। अतः एक निश्चित ताप पर गैसों की विलेयता उसके अवशोषण गुणांक पर निर्भर करती है।
एक निश्चित ताप एवं एक वायमण्डलीय दाव पर गैस की mol L-1 में विलयेता ज्ञात करने के लिए उसके अवशोषण गुणांक को 22.4 से भाग देते हैं।
प्रभावित करने वाले कारक-
- दाब का प्रभाव – हेनरी के अनुसार, गैस की विलेयता गैस पर लगने वाले दाब के समानुपाती होती है अर्थात् दाब बढ़ाने पर गैसों की विलेयता भी बढ़ जाती है।
- ताप का प्रभाव – ताप बढ़ाने पर गैस की विलेयता कम हो जाती है क्योंकि गैसों के अणुओं की गतिज ऊर्जा बढ़ जाती है।
- अशुद्धियों का प्रभाव – द्रव में घुले हुये अन्य पदार्थ जैसे-कार्बनिक पदार्थ, विद्युत् अपघट्य, धूल आदि गैस की विलेयता कम कर देते हैं।
- गैस की प्रकृति – ऐसी गैसें जो या तो विलयन में आयनित हो जाती हैं या विलायक से अभिक्रिया कर लेती हैं, वे ज्यादा विलेयशील होती हैं।
- विलायक की प्रकृति – ध्रुवीय गैसें, ध्रुवीय विलायके में तथा अध्रुवी गैसें अध्रुवी विलायक में आसानी से घुल जाती हैं।
प्रश्न 2.
रॉउल्ट के नियम की सीमाएँ लिखें।
उत्तर:
- विद्युत्-अपघट्यों के विलयनों पर रॉउल्ट का नियम लागू नहीं होता है।
- यह केवल तनु विलयनों पर लागू होता है। सान्द्र विलयन में यह विचलन प्रदर्शित करता है।
- जो पदार्थ विलयन में संगुणित या वियोजित होते हैं वे इस नियम का पालन नहीं करते हैं।
प्रश्न 3.
बेंड्स क्या है और यह किस प्रकार उत्पन्न होता है ?
उत्तर:
गहरे समुद्र में जब गोताखोर श्वास लेते हैं तब दाब अधिक होने के कारण गैसें रुधिर में अधिक मात्रा में विलेय हो जाती हैं। जब गोताखोर सतह पर आते हैं तो बाहरी दाब धीरे-धीरे कम होने लगता है। जिसके कारण घुली हुई गैसें बाहर निकल आती हैं एवं रुधिर में नाइट्रोजन के बुलबुले बन जाते हैं। यह कोशिकाओं में अवरोध उत्पन्न कर देता है और एक चिकित्सीय अवस्था उत्पन्न कर देता है जिसे बेंड्स (Bends) कहते हैं। यह अवस्था अत्यधिक पीड़ादायक एवं जानलेवा होती है।
प्रश्न 4.
ठोसों की द्रवों में विलेयता को प्रभावित करने वाले कारक लिखें।
उत्तर:
- ताप का प्रभाव – ला-शातेलिये के नियमानुसार ताप बढ़ाने पर साम्य ऊष्माशोषी अभिक्रिया की दिशा में विस्थापित हो जाता है। अतः यदि अभिक्रिया ऊष्माक्षेपी है। तो ताप बढ़ाने पर ठोसों की विलेयता द्रव में कम हो जाती है और यदि अभिक्रिया ऊष्माशोषी है तो ताप बढ़ाने पर ठोसों की विलेयता अधिक हो जाती हैं।
- दाब – ठोसों की द्रवों में विलेयता पर दाब को कोई सार्थक प्रभाव नहीं होता है क्योंकि ठोस एवं द्रव अत्यधिक असंपीड्य होते हैं।
- समान – समान को घोलता है-यदि विलेय ध्रुवीय है तो यह ध्रुवीय विलायक में घुलेगा एवं यदि विलेय अध्रुवीय है तो यह अध्रुवीय विलायक में घुलेगा।
प्रश्न 5.
द्रवों के वाष्प दाब को प्रभावित करने वाले कारक लिखें?
उत्तर:
द्रवों के वाष्प ‘दाब को प्रभावित करने वाले निम्न कारक हैं
- ताप – ताप बढ़ाने पर द्रवों को वाष्प दाब बढ़ जाता है क्योंकि अणुओं की गतिज ऊर्जा ताप बढ़ने से बढ़ जाती है।
- द्रव की प्रकृति – जिन द्रवों का अन्तराण्विक आकर्षण बल कम होता है उन द्रवों का वाष्प दाब ज्यादा होता है एवं जिन द्रवों का अन्तराण्विक आकर्षण बल ज्यादा होता है उनका वाष्प दाब कम होता है।
- श्यानता – जिन द्रवों की श्यानता ज्यादा होती है। उनका वाष्प दाब कम एवं जिन द्रवों की श्यानता कम होती है, उनका वाष्प दाब अधिक होता है।
प्रश्न 6.
हेनरी के नियम की सीमाएँ लिखें।
उत्तर:
- विलयन का दाब उच्च नहीं होना चाहिये।
- विलयन का ताप बहुत कम नहीं होना चाहिये।
- विलायक में गैस अधिक घुलनशील नहीं होनी चाहिये।
- गैस न तो विलायक के साथ रासायनिक अभिक्रिया करे, न ही विलायक में संगुणित या वियोजित हो।
प्रश्न 7.
कार्बन डाइ सल्फॉइड को ऐसीटोन में मिलाने पर विलयन धनात्मक विचलन दिखाता है क्यों?
उत्तर:
CS2 तथा ऐसीटोन से बने विलयन में विलेय- विलायक अणुओं के मध्य द्विध्रुवीय अन्योन्य क्रियाएँ विलेय-विलेय और विलायकविलायक अणुओं के मध्य अन्योन्य क्रियाओं से कमजोर होती हैं अतः विलयन धनात्मक विचलन दिखाता है।
प्रश्न 8.
ऐथेनॉल तथा ऐसीटोन का मिश्रण ऋणात्मक विचलन क्यों प्रदर्शित करता है ?
अथवा
ऐथेनॉल व ऐसीटोन का मिश्रण किस प्रकार का विचलन दिखाता है कारण दे।
उत्तर:
ऐथेनॉल तथा ऐसीटोन का मिश्रण जब बनाया जाता है तो अन्तराआण्विक हाइड्रोजन बन्ध के कारण नये आकर्षण बल उत्पन्न होते हैं तथा आकर्षण बल प्रबल हो जाते हैं जिसके कारण विलेय-विलायक अणुओं के मध्य अन्योन्य क्रियाएँ विलेय-विलेय तथा विलायक-विलायक की अपेक्षा मजबूत हो जाती है और इसी कारण ऐथेनॉल तथा ऐसीटोन का मिश्रण ऋणात्मक विचलन प्रदर्शित करता है।
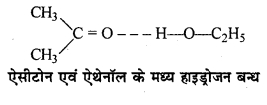
प्रश्न 9.
आदर्श एवं अनादर्श विलयन में अन्तर बताइए।
उत्तर:
आदर्श एवं अनादर्श विलयन में अन्तर

प्रश्न 10.
परासरण की जैविक महत्ता लिखें।
उत्तर:
परासरण की जैविक महत्ता – जल पौधों में परासरण की सहायता से ही जड़ों तथा पौधों के ऊपरी हिस्से तक जाता है। पौधों में कोशिकाएँ होती हैं जिनमें कोशिकाद्रव्य भरा होता है। कोशिका की दीवारें एक अर्द्ध-पारगम्य झिल्ली का कार्य करती हैं। इसी कारण जल बाहर से इन कोशिकाओं में परासरण विधि द्वारा प्रवाह करता है और जड़ एवं तने के ऊपरी हिस्से तक परासरण विधि द्वारा पहुँच जाता है।
प्रश्न 11.
विसरण एवं परासरण में अन्तर लिखें।
उत्तर:
विसरण एवं परासरण में अन्तर
विसरण
- इसमें अर्द्धपारगम्य झिल्ली का प्रयोग नहीं होता है।
- विसरण द्रव, गैस एवं विलयन में हो सकता है।
- इसको न तो रोका जा सकता है और न ही विपरीत दिशा में किया जा सकता है।
- इसमें विलेय तथा विलायक दोनों के ही अणु एक क्षेत्र से दूसरे क्षेत्र में जा सकते हैं।
परासरण
- इसमें अर्द्धपारगम्य झिल्ली का प्रयोग होता है।
- यह केवल विलयन में होता है।
- इसे बाह्य दाब लगाकर रोका जा सकता है या विपरीत दिशा में प्रवाहित किया जा सकता है।
- इंसमें केवल विलायक के अणु कम सान्द्रता वाले विलयन से अधिक सान्द्रता वाले विलयन की तरफ जाते हैं।
प्रश्न 12.
पानी में डालने पर किशमिश फूल जाती है जबकि चीनी के सान्द्र विलयन में यह सिकुड़ जाती है। क्यों ?
उत्तर:
पानी में डालने पर किशमिश परासरण के कारण फूल जाती है क्योंकि यहाँ पर विलायक के अणुओं का प्रवाह कम सान्द्रता वाले (जल) से अधिक सान्द्रता वाले (किशमिश) विलयन की तरफ होता है।
जबकि किशमिश को चीनी में डालने से किशमिश के अन्दर की सान्द्रता कम हो जाती है और विलायक के अणु किशमिश से चीनी के सान्द्र विलयन की तरफ प्रवाह करते हैं। अतः किशमिश चीनी के सान्द्र विलयन में परासरण के कारण पिचक जाती है।
प्रश्न 13.
हिमांक में अवनमन को चित्र द्वारा प्रदर्शित करें।
उत्तर:
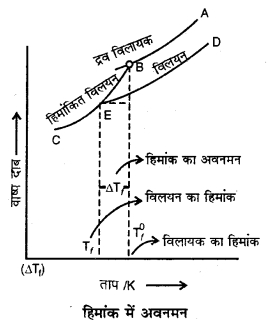
प्रश्न 14.
क्वथनांक में उन्नयन को चित्र द्वारा प्रदर्शित करें।
उत्तर:
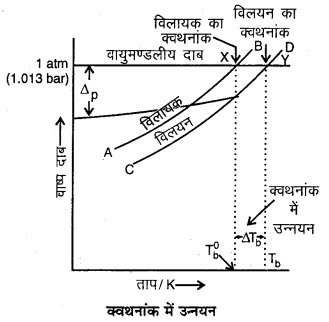
प्रश्न 15.
परासरण दाब ज्ञात करने का सूत्र स्थापित करें। (यहाँ π = परासरण दाब)
उत्तर:

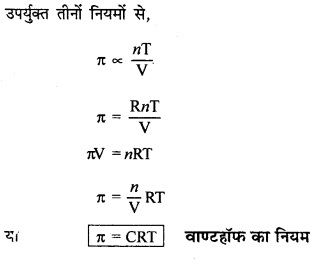
प्रश्न 16.
क्वथनांक एवं क्वथनांक में उन्नयन से आप क्या समझते हैं ?
उत्तर:
क्वथनांक – वह ताप जिस पर किसी द्रव का वाष्प दाब वायुमण्डलीय दाब के बराबर हो जाये, क्वथनांक कहलाता है।
क्वथनांक में उन्नयन – जब किसी द्रव में अवाष्पशील विलेय को डालते हैं तो उसका वाष्प दाब कम हो जाता है। अत: इस वाष्पदाब को वायुमण्डलीय दाब के बराबर करने के | लिये हमें उस द्रव को और अधिक ताप देना होगा जिससे उसका क्वथनांक बढ़ जाता है। यही क्वथनांक में उन्नयन कहलाता है।
RBSE Class 12 Chemistry Chapter 2 विलयन विस्तृत उत्तरीय प्रश्न
प्रश्न 1.
(a) विलयन की मोलरता तथा मोललता में विभेद कीजिए। इनके मानों पर ताप परिवर्तन का क्या प्रभाव पड़ता है?
(b) मोलरता तथा नॉर्मलता में सम्बन्ध प्रदर्शित कीजिए।
उत्तर:
विलयन की सान्द्रता की इकाइयाँ
किसी विलयन का संघटन उसकी सान्द्रता से व्यक्त किया जा सकता है। यहाँ सान्द्रता से तात्पर्य विलेय की उस मात्रा से है जो विलयन या विलायक की निश्चित मात्रा या आयतन में घुली हो। विलयन की सान्द्रता की इकाइयाँ निम्न प्रकार व्यक्त की जा सकती हैं।
(i) द्रव्यमान प्रतिशत (Mass Percentage; w/W) – विलेय पदार्थ के भार भागों की वह संख्या जो विलयन के 100 ग्राम भार भागों में उपस्थित हो, विलयन की द्रव्यमान प्रतिशतता कहलाती है।
द्रव्यमान % या % w/W


प्रश्न 2.
ठोस की द्रव में विलेयता को परिभाषित कीजिए। ठोस की द्रव में विलेयता किन कारकों पर निर्भर करती है?
उत्तर:
ठोसों की द्रवों में विलेयता – सभी ठोस कम या अधिक मात्रा में सभी द्रव विलायकों में विलेय होते हैं। एक ठोस की भिन्न-भिन्न विलायकों में विलेयता भिन्न-भिन्न होती है।
विलेयता – एक निश्चित ताप पर 100 g विलायक में ठोस की ग्राम में अधिकतम घुलनशील मात्रा ठोस की विलेयता कहलाती है। इस अवस्था में विलयन संतृप्त विलयन कहलाता है।
प्रश्न 3.
हेनरी का नियम लिखिए। इसके प्रमुख अनुप्रयोग तथा सीमाओं का वर्णन कीजिए।
उत्तर:
गैस की विलेयता को प्रभावित करने वाले कारक – किसी विलायक में गैस की विलेयता निम्नलिखित कारकों पर निर्भर करती है –
(i) गैस की प्रकृति – गैस जो विलायक से अभिक्रिया करती है अथवा विलयन में आयनित होती है, वह बहुत अधिक विलेयशील होती है। उदाहरणार्थ – NH3, HCl व SO2 जल में अत्यधिक विलेयशील हैं। जल में घुलकर ये NH4OH, HCl (l) व H2SO4 यौगिक बनाती है। ऑक्सीजन रुधिर में अधिक विलेयशील होती। है क्योंकि यह रुधिर के हीमोग्लोबिन से क्रिया कर लेती है। N2, O2 तथा H2 आदि गैसें अपेक्षाकृत कम विलेयशील हैं लेकिन ऐथिल एल्कोहल में अधिक विलेय होती है।
गैसों की विलेयता अवशोषण गुणांक पर भी निर्भर करती है। जिन गैसों का अवशोषण गुणांक अधिक होता है उनकी विलेयता भी अधिक होती है। 1 cm3 जल में विभिन्न गैसों का अवशोषण गुणांक का घटता क्रम निम्न प्रकार होता है –
NH3 > HCl > SO2 > H2S > CO2 > C2H2 > O2 > N2
(ii) विलायक की प्रकृति – गैस की विलेयता पर विलायक की प्रकृति के प्रभाव के संदर्भ में यह देखा गया हैं कि वे गैसें जिनमें ध्रुवीय अणु होते हैं, अध्रुवीय विलायकों की अपेक्षा, ध्रुवीय विलायक में अधिक विलेयशील होती हैं।
उदाहरण – HCl गैस, बैंजोन की अपेक्षा जल में अधिक विलेय होती है।
(iii) ताप का प्रभाव – ला-शातेलिये सिद्धान्त के अनुसार स्थिर दाब परे, ताप में वृद्धि से गैसों की विलेयता घटती है। चूंकि ताप बढ़ाने पर द्रव में गैस की अणुओं की स्थानान्तरण गतिज ऊर्जा बढ़ती है जिससे गैस के बाहर निकलने की प्रवृत्ति में वृद्धि होती है।
अपवाद- H2 व He के घुलने पर ऊष्मा का अवशोषण होता है, अतः इन गैसों की विलेयता बढ़ती है। यदि ताप में वृद्धि की जाये।
(iv) दाब का प्रभाव (हेनरी का नियम) – हम जानते हैं कि गैसों की प्रकृति दाब से बहुत अधिक प्रभावित होती है। गैसों के अन्य गुणों की भाँति इसकी विलेयता भी दाब से प्रभावित होती है। सर्वप्रथम विलियम हेनरी (William Henry, 1803) ने विभिन्न गैसों की विलेयता पर दाब का अध्ययन किया और उसने एक मात्रात्मक सम्बन्ध (quantitative relation) दिया जिसे हेनरी का नियम कहते हैं। इसके अनुसार,
स्थिर ताप पर किसी विलायक के इकाई आयतन में किसी गैस की घुली हुई मात्रा, उस द्रव की सतह पर साम्यावस्था में उस गैस द्वारा लगाए गए दाब के समानुपाती होती है।”

हेनरी नियम के अनुप्रयोग – हेनरी नियम के जहाँ उद्योगों में अनेक अनुप्रयोग हैं वहीं यह कुछ जैविक घटनाओं को समझने में भी सहायक होता है। इसके कुछ महत्वपूर्ण अनुप्रयोग निम्नानुसार हैं –
(1) सोडा – जल एवं शीतल पेयों में CO2, की विलेयता बढ़ाने के लिए बोतल को अधिक दाब पर बन्द किया जाता है।
(2) गहरे समुद्र में श्वास लेते हुए गोताखोरों को अधिक दाब पर गैसों की अधिक घुलनशीलता का सामना करना पड़ सकता है। अधिक बाहरी दाब के कारण श्वास के साथ ली गई वायुमण्डलीय गैसों की विलेयता रुधिर में अधिक हो जाती है। जब गोताखोर सतह की ओर आते हैं तो बाहरी दाब धीरे-धीरे कम होने लगता है। इसके कारण घुली हुई गैसे बाहर निकलती हैं, इससे रुधिर में नाइट्रोजन के बुलबुले बन जाते हैं। ये केशिकाओं में अवरोध उत्पन्न कर देते हैं और एक चिकित्सीय अवस्था उत्पन्न कर देते हैं जिसे बेंड्स (Bends) कहते हैं। यह अत्यधिक पीड़ादायक एवं जानलेवा होता है। बेंड्स से तथा नाइट्रोजन की रुधिर में अधिक मात्रा के जहरीले प्रभाव से बचने के लिए, गोताखोरों द्वारा श्वास लेने के लिए उपयोग किए जाने वाले टैंकों में हीलियम मिलाकर तनु की गई वायु को भरा जाता है (11-7% हीलियम, 56-2% नाइट्रोजन तथा 32:1% ऑक्सीजन)।
(3) अधिक ऊँचाई वाली जगहों पर ऑक्सीजन का आंशिक दाब सतही स्थानों से कम होता है; अत: इन जगहों पर रहने वाले लोगों एवं आरोहकों के रुधिर और ऊतकों में ऑक्सीजन की सान्द्रता निम्न (low) हो जाती है। इसके कारण आरोहक कमजोर हो जाते हैं और स्पष्टतया सोच नहीं पाते। इन लक्षणों को ऐनॉक्सिया (Anoxia) कहते हैं।
हेनरी नियम की सीमायें हेनरी नियम की निम्न सीमायें हैं –
- ताप बहुत कम नहीं होना चाहिए।
- दाब का मान अत्यधिक नहीं होना चाहिए।
- गैस की विलेयता किसी विलायक में कम होनी चाहिए।
- गैस की आण्विक अवस्था द्रव व गैसीय दोनों अवस्थाओं में समान होनी चाहिए अर्थात् गैसों का न तो संयोजन होना चाहिये न ही वियोजन।
प्रश्न 4.
वाष्पशील विलेय युक्त विलयन के लिए रॉउल्ट का नियम लिखिए।
उत्तर:
रॉउल्ट का नियम
फ्रेंच रसायनज्ञ फ्रेंसियस मार्टे रॉउल्ट (1986) ने सर्वप्रथम वाष्प दाब अवनमन और विलयन की सान्द्रता के मध्य मात्रक सम्बन्ध स्थापित किया –
प्रश्न 5.
अणुसंख्य गुणों से आप क्या समझते हैं? परासरण तथा परासरण दाब को संक्षेप में समझाइए।
उत्तर:
विलयनों के अणुसंख्यक गुणधर्म
विलयन के वे गुण, जो विलयन के निश्चित आयतन में उपस्थित विलयनों के मोलों की संख्या या अणुओं की संख्या पर आधारित होते हैं, विलयन के अणुसंख्यक गुण कहलाते हैं। अणुसंख्यक गुण विलेय के रासायनिक गुणों या प्रकृति पर निर्भर नहीं होते हैं, बल्कि ये अणुओं की संख्या पर निर्भर होते हैं; जैसे- चीनी या यरिया के एक मोल को यदि 100 mL जल में घोलें तो प्राप्त विलयनों का सदैव एक-सा क्वथनांक में उन्नयन या वाष्प दाब में अवनमन होगा। विलयन में अणुसंख्यक गुणधर्म व कणों या अणुओं की संख्या इन गुणों में आयन भी कणों के समान व्यवहार करते हैं।
अणुसंख्यक गुणों के नाम कुछ मुख्य अणुसंख्यक गुण इस प्रकार हैं –
- विलायक के वाष्प दाब का अवनमन
- विलायक के क्वथनांक का उन्नयन
- विलायक के हिमांक का अवनमन
- विलायक का परासरण दाब।
परासरण – “जब निम्न सान्दता वाले विलयन से विलायक अर्द्धपारगम्य झिल्ली द्वारा उच्च सान्दता वाले विलयन की ओर प्रवाहित हो, तो इस घटना को परासरण कहते हैं।” परासरण की प्रक्रिया को समझाने के लिए हम उल्टी थिसिल कीप के उपकरण को लेते हैं। इस कीप के मुख पर अर्द्धपारगम्य झिल्ली को बाँध लेते हैं। इसे (चित्र 2.8) में दिखाया गया है अर्द्धपारगम्य झिल्ली केवल विलायक के कणों को ही गुजरने देती है, विलेय के अणु झिल्ली में से नहीं गुजरते हैं। कीप में कॉपर सल्फेट (CuSO4) का सान्द्र विलयन भर कर, इसे जलयुक्त बीकर में रख देते हैं।
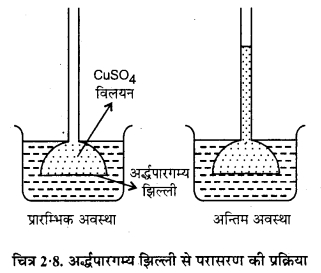
परासरण दाब – विलयन पर लगाया गया बाह्य दाब जो अर्द्धपारगम्य झिल्ली में विलायक के अणुओं का प्रवाह रोकने तथा तल में साम्य स्थापित करने के लिए आवश्यक होता है परासरण दाब कहलाता है।
या
परासरण दाब वह दाब है जिसे शुद्ध विलायक पर से कम करने पर उसका वाष्प दाब कम होकर विलयन के वाष्प दाब के बराबर हो जाएं या वह आधिक्य दाब जिसे विलयन पर लगाया जाए ताकि विलयन का वाष्प दाब विलायक के वाष्प दाब के समान हो जाए।
परासरण दाब को हम (चित्र 2.9) में दिखाये गये उपकरण पर प्रयोग द्वारा समझ सकते हैं।
प्रयोग के लिए काँच के एक पात्र को अर्द्धपारगम्य झिल्ली की सहायता से दो भागों में बाँट देते हैं। एक भाग में काँच की एक संकरी नली लगाते हैं जिससे विलायक भरते हैं। जबकि दूसरे भाग में एक चौड़ी नली लगाते हैं जिसमें जल रोकने वाला घर्षण रहित पिस्टन लगा होता है। विलयन इसी भाग में लिया जाता है। प्रक्रिया के शुरू होने पर विलायक के अणु अर्द्धपारगम्य झिल्ली द्वारा विलयन में जाने की कोशिश करेंगे जिससे पिस्टन ऊपर की ओर जायेगा। जबकि संकरी नली में जल का स्तर गिरेगा।